Maio
Documentos da Sputnik ainda são insuficientes, informa Anvisa aos estados que voltaram a pressionar agência por liberação da vacina russa
Postado às 9:38 Hs
A Anvisa (Agência Nacional de Vigilância Sanitária) informou nesta sexta-feira (7) que documentos adicionais enviados pelos governos da Bahia, Maranhão e Sergipe para apoiar o pedido de autorização para importação da vacina russa contra covid-19 Sputnik V são insuficientes, e que segue aguardando os esclarecimentos necessários para realizar uma nova análise do imunizante.
“Após avaliação, verificou-se que os novos documentos apresentados não cumprem o requisito alusivo à apresentação do relatório técnico de análise da autoridade sanitária estrangeira”, disse a Anvisa em nota.
“Em razão disso, os Estados foram comunicad os que os processos seguem em diligência até que os esclarecimentos necessários sejam capazes de subsidiar a análise dos pedidos de importação”, acrescentou.
os que os processos seguem em diligência até que os esclarecimentos necessários sejam capazes de subsidiar a análise dos pedidos de importação”, acrescentou.
A Anvisa rejeitou na semana passada pedido de governos estaduais para importar a Sputnik V, alegando falta de informações suficientes para garantir a segurança, a qualidade e a eficácia do imunizante. A agência citou a presença de adenovírus replicante na vacina como um dos principais pontos críticos observados pela área técnica na análise do imunizante.
Os desenvolvedores russos da vacina, assim como os Estados brasileiros que buscam a importação, negam que haja qualquer problema com a Sputnik V, que já está em aplicação em diversos países.
“A agência segue na busca de informações referentes à vacina Sputnik V que resguardem os aspectos mínimos de qualidade, segurança e eficácia para uso na população brasileira”, acrescentou a Anvisa na nota desta sexta.
R7
abr
Anvisa trata acusações da Sputnik como ‘ataque a um país’ e expõe diálogos
Postado às 20:59 Hs
A Anvisa (Agência Nacional de Vigilância Sanitária) entrou com um recurso ao STF (Supremo Tribunal Federal) pedindo que a Corte suspenda o prazo para emitir um parecer sobre a importação temporária da  até que o órgão obtenha dados suficientes sobre o imunizante. A Anvisa é representada no processo pela Advocacia-Geral da União (AGU).
até que o órgão obtenha dados suficientes sobre o imunizante. A Anvisa é representada no processo pela Advocacia-Geral da União (AGU).
O recurso da agência questiona uma decisão do ministro Ricardo Lewandowski, que deu um prazo de 30 dias, contados a partir de 29 de março, para a Anvisa decidir sobre a liberação da compra de doses da vacina russa contra a Covid-19 pelo estado do Maranhão. Nesta semana, a liminar de Lewandowski foi estendida ao governo do Ceará.
Recurso
No recurso, a Anvisa afirma que há necessidade de “uma decisão administrativa fundamentada voltada ao melhor interesse público”. O argumento é de que as informações disponíveis para análise são insuficientes. “Até o presente momento, a Anvisa obteve informações apenas da autoridade sanitária argentina (Anmat), por meio do recebimento de Informe, referente à vacina Sputnik V, o qual ainda está submetido à avaliação pelas áreas técnicas da Agência”, diz a agencia reguladora.
Segundo a Anvisa, “no caso da Sputnik V, o relatório técnico da agência sanitária respectiva não foi publicizado e, mesmo com as diligências e pedidos feitos, inclusive junto à Autoridade Russa, não foi possível obtê-lo até o momento”.
“O caso em questão, portanto, é atípico, pois o relatório da autoridade russa para concessão do registro da Sputnik V não é público e não há dados em outras fontes capazes de trazer as informações sobre qualidade, eficácia e segurança para o processo de importação em questão”, afirmou ao STF.
Sputnik V
A agência nacional já recusou, em outra oportunidade, o uso da Sputnik V no Brasil, alegando falta de documentos. Nesta semana, integrantes do órgão estão na Rússia, visitando fábricas e centros de pesquisa envolvidos na elaboração do imunizante no país.
A argumentação central em favor da liberação da Sputnik V é a autorização da vacina russa em outros países cujas agências reguladoras são consideradas de trabalho fidedigno pela legislação brasileira.
A vacina já foi adquirida pelos governadores de estados do Norte e Nordeste e também pelo governo federal. Recentemente, a vacina foi tema de uma ligação entre o presidente Jair Bolsonaro (sem partido) e o presidente da Rússia, Vladimir Putin.
CNN BRASIL
abr
Coquetel aprovado para tratamento da Covid reduz internações e mortes em 70%, diz Anvisa
Postado às 21:28 Hs
O ministro do Supre mo Tribunal Federal (STF) Ricardo Lewandowski definiu, hoje, prazo até o fim deste mês para que a Agência Nacional de Vigilância Sanitária (Anvisa) decida sobre a “importação excepcional e temporária” de doses da vacina Sputnik V.
mo Tribunal Federal (STF) Ricardo Lewandowski definiu, hoje, prazo até o fim deste mês para que a Agência Nacional de Vigilância Sanitária (Anvisa) decida sobre a “importação excepcional e temporária” de doses da vacina Sputnik V.
O ministro tomou a decisão em uma ação protocolada pelo governo do Maranhão, que diz ter negociado 4,5 milhões de doses da vacina produzida pelo Instituto Gamaleya, da Rússia.
Na decisão, Lewandowski determina que a decisão seja tomada em até 30 dias, a contar do último dia 29 de março. Se forem incluídos no prazo os fins de semana e feriados, a data limite será o dia 28 de abril.
Lewandowski diz que, se o prazo for descumprido, o Maranhão fica automaticamente autorizado a importar e distribuir as doses da Sputnik V, “sob sua exclusiva responsabilidade, e desde que observadas as cautelas e recomendações do fabricante e das autoridades médicas”.
A Anvisa já recebeu dois pedidos de autorização de uso emergencial da Sputnik V – o primeiro foi apresentado ainda em janeiro, mas a agência considerou que faltavam documentos. O segundo pedido foi feito em 26 de março, mas a Anvisa ainda não deu resposta e suspendeu a análise.
abr
Anvisa convoca 11 governadores para discutir problemas em liberação de vacina russa
Postado às 11:42 Hs
A Agência Nacional de Vigilância Sanitária (Anvisa) convocou os governadores dos 11 Estados interessados em importar a vacina russa Sputnik V para explicar em detalhes as dificuldades que o órgão regulador vem enfrentando para avançar com a autorização para o uso emergencial do imunizante no país.
A proposta inicial da agência é que a reunião aconteça na terça-feira (6), mas a confirmação vai depender das agendas dos governadores. Manifestaram interesse em comprar as vacinas os governadores de Acre, Bahia, Rio Grande do Norte, Maranhão, Mato Grosso, Piauí, Ceará, Pernambuco, Pará, Sergipe e Rondônia.
 A Agência Nacional de Vigilância Sanitária (Anvisa) informou que, até o momento, os dados públicos de notificações do uso de vacinas contra covid-19 no país não indicam qualquer relação das vacinas com eventos adversos graves ou mortes. De acordo com a Anvisa, não houve alteração na relação de risco e benefício dos produtos.
A Agência Nacional de Vigilância Sanitária (Anvisa) informou que, até o momento, os dados públicos de notificações do uso de vacinas contra covid-19 no país não indicam qualquer relação das vacinas com eventos adversos graves ou mortes. De acordo com a Anvisa, não houve alteração na relação de risco e benefício dos produtos.
Em nota, a agência reguladora explicou que a avaliação benefício-risco leva em conta um conjunto grande de informações e os registros informados pelos usuários são apenas uma dessas fontes. As outras envolvem os relatórios de segurança das fabricantes, os sinais de segurança gerados pelo modelo matemático da Organização Mundial da Saúde (OMS), a troca de informações com outras autoridades regulatórias e a discussão em grupos de especialistas.
“Até o momento, não há nenhum caso de óbito conhecido que tenha relação estabelecida com o uso das vacinas para covid-19 autorizadas no país. As vacinas em uso no Brasil são consideradas seguras”, informou a agência. “Já é esperado que pessoas venham a óbito por outros motivos de saúde e mesmo por causas naturais, tendo em vista a taxa de mortalidade já conhecida para cada faixa etária da população brasileira”, completou.
jan
Anvisa aprova pedido de uso de 4,8 milhões de doses em novo lote da CoronaVac
Postado às 17:00 Hs
jan
Anvisa marca reunião com União Química para tratar de autorização da Sputnik V
Postado às 8:39 Hs
jan
Governo Federal lança nesta 4ª feira campanha “Brasil imunizado, somos uma só nação”
Postado às 9:22 Hs
jan
Reunião que avaliará uso emergencial de vacinas será transmitida ao vivo e deve durar 5h, diz Anvisa
Postado às 17:54 Hs
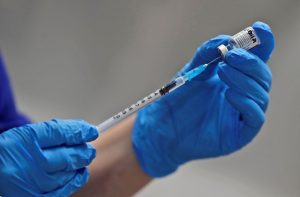
Foto: Frank Augstein/Pool/Reuters/Arquivo
A Anvisa (Agência Nacional de Vigilância Sanitária) informou hoje (16) que a reunião marcada para amanhã (17) com o intuito de avaliar os pedidos de uso emergencial das vacinas contra a covid-19 deve durar pelo menos cinco horas. Os trabalhados serão transmitidos ao vivo pela internet e vão começar às 10h.
Dois imunizantes estão na pauta da Anvisa: a CoronaVac, de origem chinesa e fabricada e desenvolvida pelo Instituto Butantan (SP); e a da Fiocruz, que é resultante de estudos da Universidade de Oxford, na Inglaterra, em parceria com o laboratório AstraZeneca.
Além da live disponibilizada pelos canais de comunicação da Anvisa, emissoras de TV anunciaram que também vão transmitir a reunião.
Responsável pela liberação de imunizantes e medicamentos no Brasil, a Anvisa, a Agência Nacional de Vigilância Sanitária, se reúne para analisar os dados de relatório elaborado pela área técnica sobre os dois pedidos. Após a análise, a diretoria da agência definirá, por meio de votação, se libera ou não a aplicação dos imunizantes.
A data da reunião corresponde ao último dia do prazo definido para analisar pedidos de uso emergencial de vacinas.
Caberá a cinco membros da Diretoria Colegiada da Anvisa a autorização de uso emergencial das vacinas: Antônio Barra Torres (diretor-presidente); Meiruze Sousa Freitas; Cristiane Rose Jourdan Gomes; Romison Rodrigues Mota; e Alex Machado Campos.
UOL
jan
Se Anvisa aprovar uso da Coronavac, vacinação pode ser antecipada, diz Doria
Postado às 9:24 Hs
dez
Ministério da Saúde prevê iniciar vacinação cinco dias após aval da Anvisa e entrega das doses
Postado às 21:49 Hs
O Ministério da Saúde informou ao Supremo Tribunal Federal (STF), nesta terça-feira (15), que o governo prevê iniciar a vacinação contra a Covid-19 em até cinco dias após o registro ou
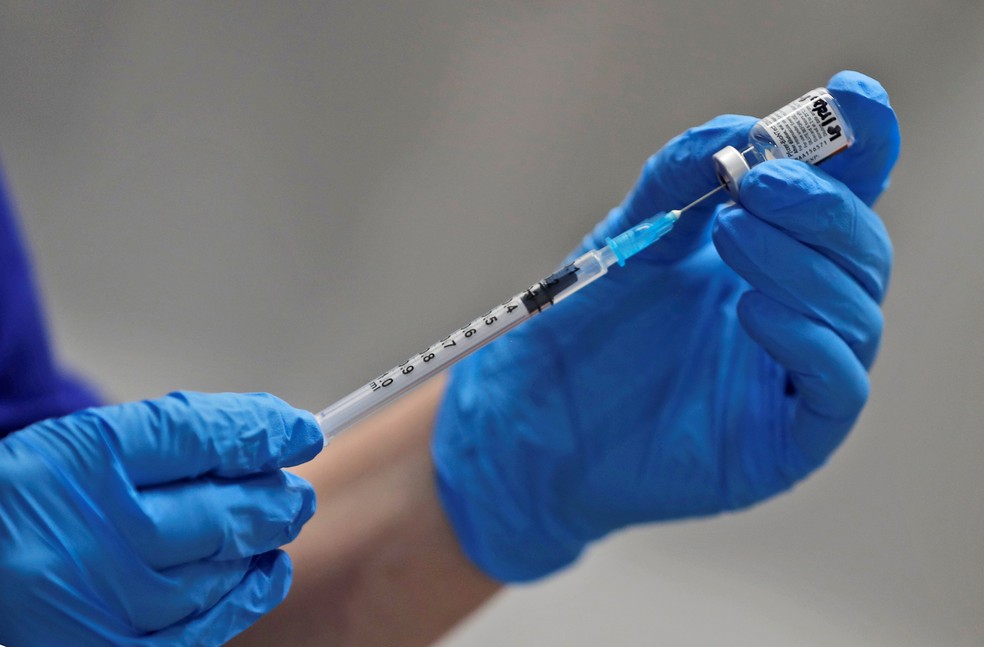
Foto: Frank Augstein/Pool/Reuters/Arquivo
autorização das doses pela Agência Nacional de Vigilância Sanitária (Anvisa) e a entrega dos primeiros lotes.
Ainda de acordo com esse novo documento, a vacinação no Brasil deve ser concluída em 16 meses – quatro meses para vacinar todos os grupos prioritários e, em seguida, 12 meses para imunizar a “população em geral”.
A informação foi entregue ao STF pela Advocacia-Geral da União (AGU) em resposta a um pedido do ministro Ricardo Lewandowski, que pediu dados complementares sobre o plano de imunização enviado ao Supremo na última sexta (11). Lewandowski é relator de duas ações sobre o tema.
No domingo (13), o ministro determinou que o ministro Eduardo Pazuello apresentasse a previsão de início e término do plano, além de detalhar suas fases de implantação.
O documento protocolado pela AGU não tem datas precisas – o governo reafirma que isso só será definido quando a Anvisa aprovar o uso das vacinas no Brasil.
A Agência Nacional de Vigilância Sanitária (Anvisa) estima que poderá avaliar e conceder autorização emergencial de vacinas contra a covid-19 em até 10 dias para empresas que cumpram os requisitos fixados. Esta modalidade de permissão foi estabelecida pelo órgão para permitir uma análise mais rápida em condições especiais de imunização diante do cenário de pandemia.
No início do mês, a Anvisa divulgou o guia de critérios e procedimentos para a aprovação de autorizações emergenciais para vacinas em caráter experimental contra a covid-19.
A permissão especial poderá ser fornecida para vacinas que estejam em estudo no Brasil na chamada Fase 3, em que a eficácia e a segurança são analisadas. Nesse caso, as vacinas serão destinadas a programas de governo, não podendo ser comercializadas pelas empresas que obtiveram a permissão.
Apenas as empresas que estão desenvolvendo as vacinas poderão solicitar a autorização na Anvisa. Deve ser comprovada a capacidade de fabricar ou de importar a substância. As companhias interessadas em tal alternativa deverão fazer antes uma reunião com a equipe da Anvisa, que é chamada de “pré-submissão”. Será preciso também já ter aprovado na Anvisa um dossiê de desenvolvimento clínico.
















 5.953.778 VISITAS
5.953.778 VISITAS